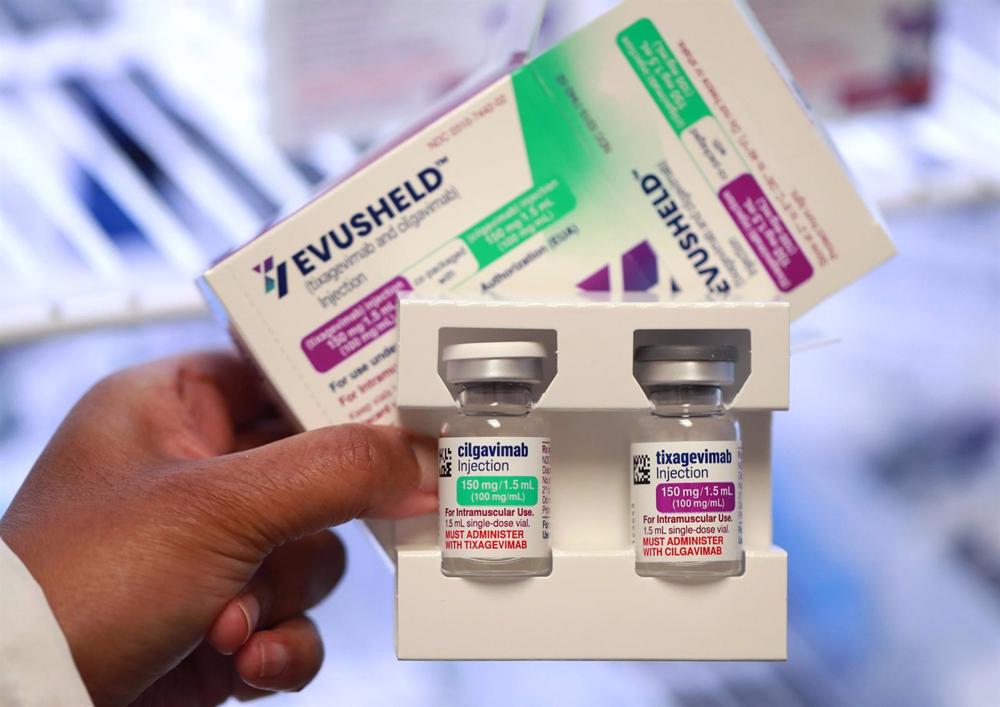
La Food and Drug Administration (FDA) statunitense ha dichiarato venerdì che la variante XBB.1.5 del coronavirus è probabilmente resistente al farmaco COVID-19 «Evusheld» di AstraZeneca.
Secondo l’FDA, l’antivirale dell’azienda farmaceutica britannica potrebbe non fornire una protezione contro lo sviluppo di COVID-19 per i soggetti che lo ricevono e sono successivamente esposti alla nuova variante.
Evusheld era l’ultimo anticorpo della sua classe ancora autorizzato negli Stati Uniti per prevenire l’infezione in individui ad alto rischio, poiché tutti gli altri farmaci erano stati esclusi a causa dell’alta probabilità che non proteggessero dalle nuove varianti.
Le terapie anticorpali sono state essenziali per trattare e prevenire le malattie in circa sette milioni di americani immunocompromessi per i quali i vaccini e gli antivirali possono essere meno efficaci, secondo Bloomberg.
Tuttavia, con la mutazione del virus COVID-19, gli anticorpi sono stati eliminati dal mercato uno dopo l’altro.
Attualmente, XBB.1.5, che proviene da Omicron, rappresenta il 28% di tutte le varianti in circolazione negli Stati Uniti, secondo i dati della FDA.
Il Direttore Generale dell’Organizzazione Mondiale della Sanità (OMS) Tedros Adhanom Ghebreyesus ha dichiarato che l’agenzia sanitaria internazionale sta valutando il rapido aumento della variante XBB.1.5 negli Stati Uniti e in altri 24 Paesi.
Tedros si è detto «molto preoccupato» per l’attuale quadro epidemiologico della COVID-19, «sia per l’intensa trasmissione in varie parti del mondo sia per la rapida diffusione di una sottovariante ricombinante».
A questo proposito, ha assicurato che l’OMS «sta monitorando e valutando attentamente il rischio di questa sottovariante e riferirà di conseguenza» sui nuovi dati.
Fonte: (EUROPA PRESS)






