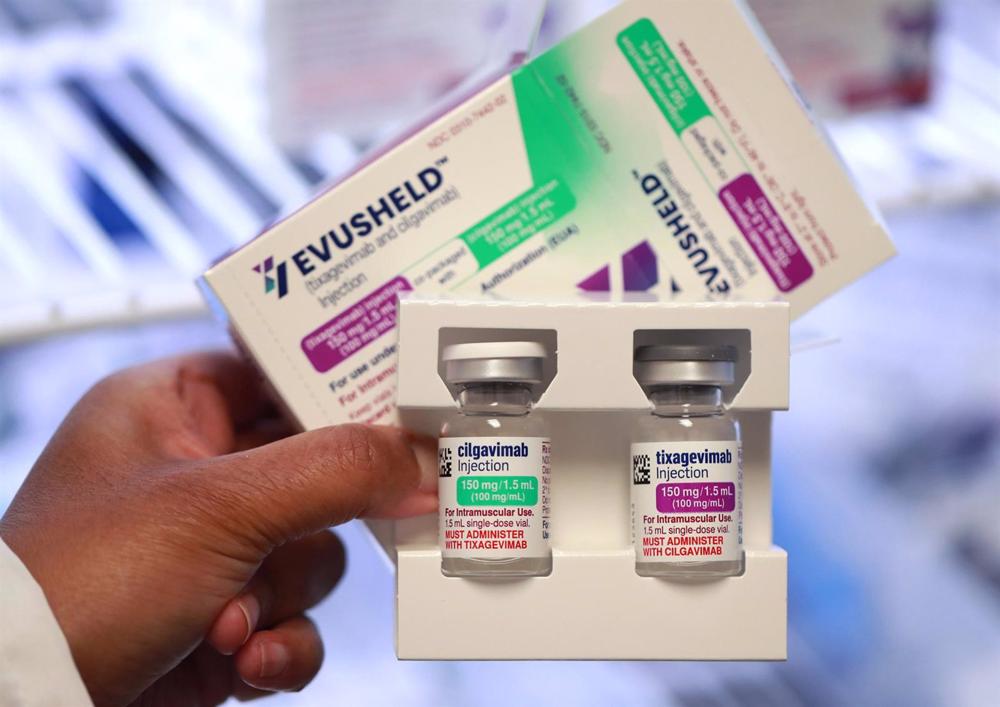
Die US Food and Drug Administration (FDA) erklärte am Freitag, dass die XBB.1.5-Variante des Coronavirus wahrscheinlich gegen das COVID-19-Medikament «Evusheld» von AstraZeneca resistent ist.
Nach Angaben der FDA bietet das Virostatikum des britischen Arzneimittelherstellers möglicherweise keinen Schutz vor der Entwicklung von COVID-19 für Personen, die es erhalten und anschließend der neuen Variante ausgesetzt sind.
Evusheld war der letzte Antikörper seiner Klasse, der in den USA noch zur Verhinderung von Infektionen bei Hochrisikopersonen zugelassen war, da alle anderen Medikamente aufgrund der hohen Wahrscheinlichkeit, dass sie nicht vor neuen Varianten schützen würden, ausgeschlossen worden waren.
Laut Bloomberg sind Antikörpertherapien für die Behandlung und Vorbeugung von Krankheiten bei etwa sieben Millionen immungeschwächten Amerikanern, für die Impfstoffe und Virostatika möglicherweise weniger wirksam sind, von wesentlicher Bedeutung.
Da das COVID-19-Virus jedoch mutiert ist, hat es einen Antikörper nach dem anderen vom Markt genommen.
Derzeit macht XBB.1.5, das von Omicron stammt, nach Angaben der FDA 28 Prozent aller in den USA zirkulierenden Varianten aus.
Der Generaldirektor der Weltgesundheitsorganisation (WHO), Tedros Adhanom Ghebreyesus, erklärte, dass die internationale Gesundheitsbehörde den raschen Anstieg der XBB.1.5-Variante in den USA und 24 anderen Ländern untersucht.
Tedros sagte, er sei «sehr besorgt» über das aktuelle epidemiologische Bild von COVID-19, «sowohl wegen der intensiven Übertragung in verschiedenen Teilen der Welt als auch wegen einer sich schnell ausbreitenden rekombinanten Subvariante».
In diesem Zusammenhang versicherte er, dass die WHO «das Risiko dieser Subvariante genau beobachtet und bewertet und über neue Daten entsprechend berichten wird».
Nachrichtenquelle: (EUROPA PRESS)






